Cigarros eletrônicos inteligentes com nomes de cartas de advertência da FDA: envolvendo 6 marcas, incluindo FUME, Craftbox, North Vape, etc.
Deixe um recado
Cartas de advertência da FDA nomeiam 'cigarros eletrônicos inteligentes': envolvendo 6 marcas, incluindo FUME, Craftbox, North Vape, etc.
2Firsts descobriu, através da classificação do último lote de cartas de advertência divulgadas pela FDA em 30 de outubro, que este incidente envolve seis marcas de cigarros eletrônicos, nomeadamente FUME, Craftbox, North Vapor, Posh, Halo Vapor e Swype.
Em 31 de outubro, a Two Up 2Firsts informou que a Food and Drug Administration (FDA) dos EUA emitiu cartas de advertência a nove varejistas on-line e um fabricante, acusando-os de vender cigarros eletrônicos inteligentes não autorizados (clique para ler o artigo). Duas ou duas primeiras descobertas, através da classificação de cartas de advertência da FDA, que esta carta de advertência envolve seis marcas de cigarros eletrônicos, nomeadamente FUME, Craftbox, North Vapor, Posh, Halo Vapor e Swype.
Dois ou dois primeiros observaram que nas dez cartas de advertência da FDA, a FDA descreveu "esses rótulos ou anúncios de produtos podem atrair jovens ao imitar smartphones ou outras tecnologias inteligentes" e "podem atrair adolescentes ao imitar produtos de jogos", e chamaram esses produtos de " muito preocupante".
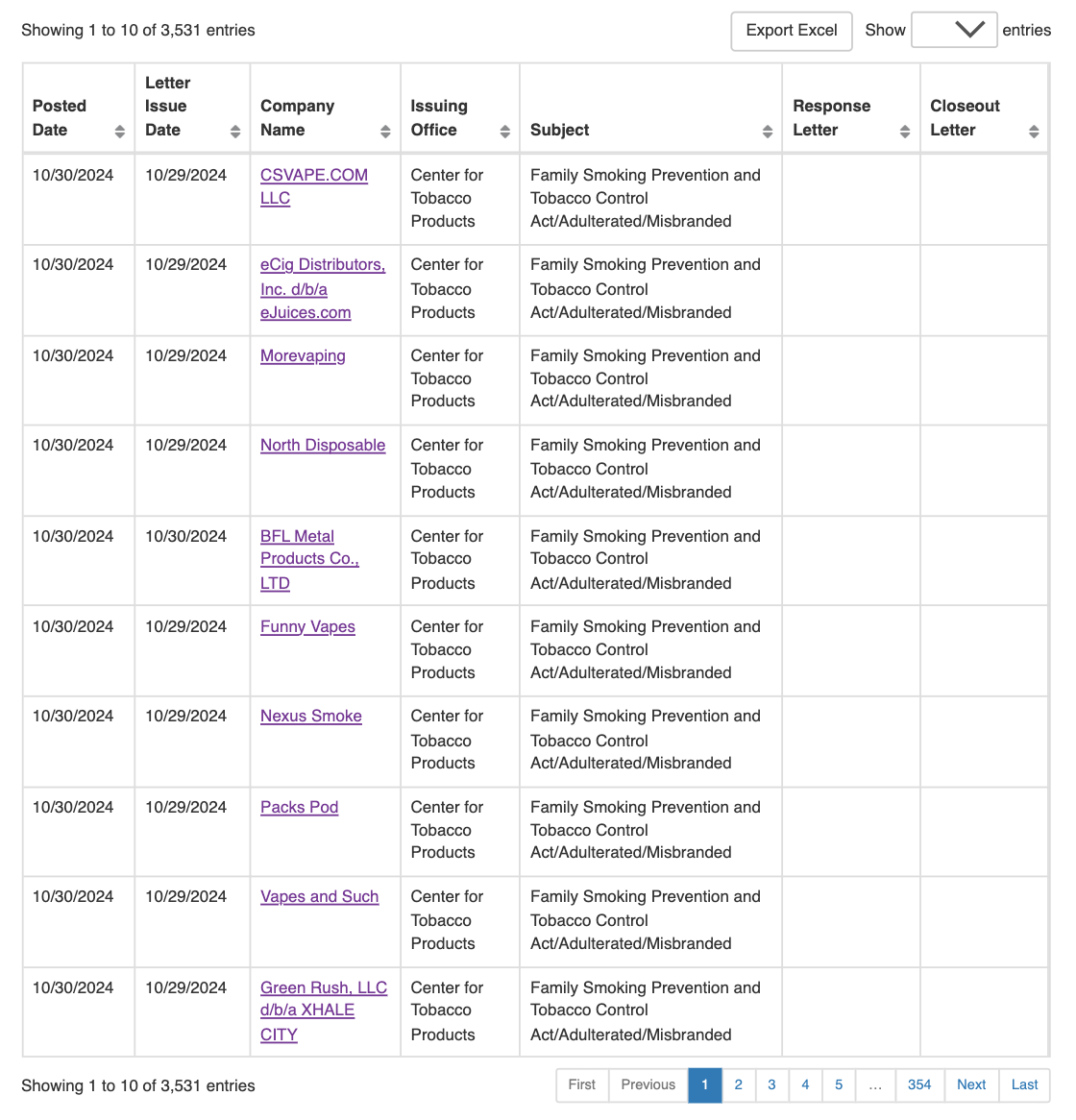
Carta de advertência emitida pela FDA|Fonte da imagem: FDA
A seguir está uma lista de marcas e seus produtos mencionados em duas cartas de advertência da FDA compiladas pela Up to 2Firsts.
FUMO
Seu produto WeFume Vape 30K Puffs foi mencionado três vezes na carta de advertência.
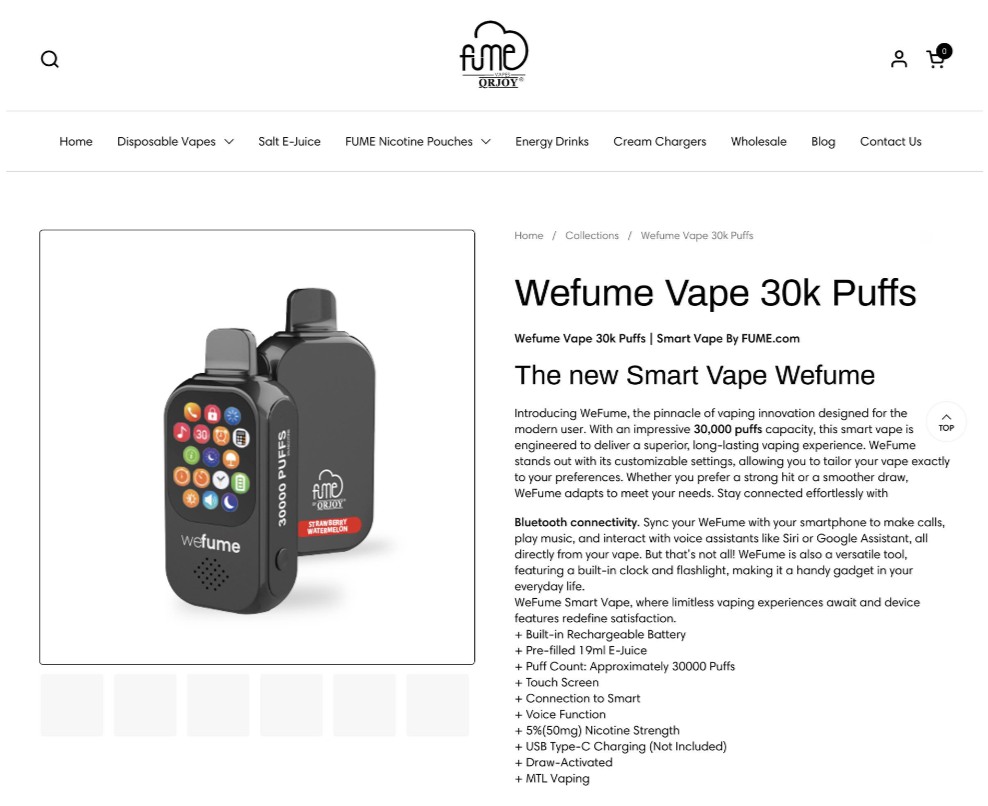
Fonte da imagem WeFume 30K Puff: Fume
Caixa de artesanato
O cigarro eletrônico descartável Craftbox V-Touch 30k Puff Smart é recomendado 4 vezes na notificação, o cigarro eletrônico descartável Craftbox V-Play 20K Puff é recomendado 5 vezes, o cigarro eletrônico descartável Craftbox V-Touch 30000 Puff Phone Call é recomendado 1 vez

Fonte da imagem: FDA
Vape Norte
Seu produto North South Connect 35K Puffs Phone Descartável Vape foi mencionado duas vezes na carta de advertência, South Connect 35K Descartável Vape Bluetooth 900mAh foi mencionado uma vez.

Fonte da imagem: FDA

Fonte da imagem: FDA
Elegante
Seus produtos, Posh Xtron 30000 Descartável Vape e Posh Pro Max 30000, foram mencionados uma vez cada na carta de advertência.

Fonte da imagem: FDA
Halo Vapor
Seu produto Halo Vapor Synix 30K foi mencionado duas vezes na carta de advertência.

Fonte da imagem: FDA
Swype
Seu produto Swype 30K Descartável Vape foi mencionado uma vez na carta de advertência.

Fonte da imagem: site do revendedor vapezilla
De acordo com a divulgação de informações da FDA, quando a FDA descobrir o que considera ser uma violação grave dos requisitos federais, notificará as partes relevantes.
Esta notificação geralmente assume a forma de uma carta de advertência. Cartas de advertência apontarão questões como práticas de produção inadequadas, problemas com a promoção da eficácia do produto ou instruções de uso incorretas. Esta carta oferece uma oportunidade para empresas ou indivíduos abordarem questões da FDA e solicitarem uma resposta dentro de um determinado período de tempo. A resposta pode incluir um plano corretivo e, em seguida, a FDA fará uma inspeção para garantir que as medidas corretivas sejam suficientes.
Se uma empresa ou indivíduo discordar da opinião da FDA, eles terão a oportunidade de fornecer à FDA suas razões e informações de apoio. Estas comunicações e outras ações entre a FDA e o destinatário da carta podem alterar o status regulatório das questões discutidas na carta.
Em 30 de outubro de 2024, o FDA aprovou 34 produtos e dispositivos para cigarros eletrônicos. A agência mantém um folheto de página única para impressão que lista todos os produtos de cigarros eletrônicos autorizados, que os varejistas podem revisar para determinar quais produtos podem ser comercializados e vendidos legalmente nos Estados Unidos. As entidades que fabricam, importam, vendem ou distribuem cigarros eletrónicos sem a necessária autorização pré-comercialização enfrentarão riscos de aplicação.







